вҖңзҢ«жҠ“иҖҒйј пјҢеӨ©з»Ҹең°д№үвҖқпјҢе…¶е®һеңЁжҲ‘们иә«дҪ“еҶ…пјҢе…Қз–«з»Ҷиғһд№ҹжҳҜиҝҷж ·жҠ“жҚ•зҷҢз»Ҷиғһзҡ„гҖӮ
дёҚиҝҮиҖҒйј еҸҲиғҪз”ҹеҸҲзӢЎзҢҫпјҢиҷҪ然еҠӘеҠӣзҡ„зҢ«еҫҲе°ҪиҒҢпјҢеҚҙд№ҹдјҡжңүеӨұзҲӘзҡ„ж—¶еҖҷгҖӮзҷҢз»Ҷиғһд№ҹжҳҜеҰӮжӯӨпјҢеңЁдёҚж–ӯзҡ„еҲҶиЈӮиҝӣеҢ–дёӯпјҢеӯҰдјҡдәҶйҖғйҒҝе…Қз–«з»Ҷиғһзҡ„зӣ‘и§ҶпјҢиў«з§°дёәгҖҢе…Қз–«йҖғйҖёгҖҚгҖӮ
е…ҲжқҘз®ҖеҚ•и§ЈйҮҠдёҖдёӢе…Қз–«з–—жі•зҡ„еҺҹзҗҶпјҡдәәдҪ“еҶ…е…Қз–«зі»з»ҹзҡ„дё»иҰҒжҲҗе‘ҳжҳҜзҷҪз»ҶиғһпјҢдҪҶд№ҹеҲҶдёәеҫҲеӨҡз§ҚпјҢжҜ”еҰӮе…¶дёӯе°ұжңүвҖңзғӯеҝғеёӮж°‘вҖқзҷҪз»Ҷиғһе’ҢвҖңй»‘зҢ«иӯҰй•ҝвҖқTз»Ҷиғһд№ӢеҲҶпјҢдёҖиҲ¬з»ҶиҸҢжҲ–з—…жҜ’е…ҘдҫөдҪ“еҶ…пјҢзҷҪз»Ҷиғһдјҡе‘јеҸ«Tз»Ҷиғһжҗһе®ҡпјҢеҗҢж—¶еҰӮжһңTз»ҶиғһеңЁиғңеҲ©еҗҺд»Қ然еҶІеҠЁпјҢзҷҪз»Ҷиғһд№ҹиғҪжҺ§еҒңе®ғпјӣдёҚиҝҮпјҢзҷҢз»ҶиғһжҳҜдәәдҪ“еҶ…жӯЈеёёз»ҶиғһеҸҳејӮпјҢжҳҜвҖңеҶ…й¬јвҖқпјҢе®ғд№ҹеӯҰдјҡдәҶжҖҺж ·жҺ§еҒңTз»ҶиғһпјҢиҝҷж—¶пјҢе°ұйңҖиҰҒйҖҡиҝҮд»ҘPD-1 е…Қз–«жЈҖжҹҘзӮ№жҠ‘еҲ¶еүӮдёәд»ЈиЎЁзҡ„е…Қз–«з–—жі•пјҢејәеҢ–Tз»ҶиғһпјҢиҜҶеҲ«еҮәзҷҢз»Ҷиғһ并ж¶ҲзҒӯе®ғгҖӮ
еңЁж—ўеҫҖз ”з©¶дёӯпјҢжӣІеҰҘзҸ еҚ•жҠ—зӯүжҠ—HER2еҚ•жҠ—иҒ”еҗҲPD-1/L1жҠ‘еҲ¶еүӮжІ»з–—HER2йҳіжҖ§д№іи…әзҷҢпјҢжүҖжҳҫзӨәзҡ„з–—ж•Ҳж—¶еҘҪж—¶еқҸпјҢ并дёҚжҳҜеҫҲзЁіе®ҡ[1]гҖӮ
иҝ‘ж—ҘпјҢдёӯеұұеӨ§еӯҰеӯҷйҖёд»ҷзәӘеҝөеҢ»йҷўзҡ„з ”з©¶еӣўйҳҹпјҢеҹәдәҺдёҖйЎ№иҜ„дј°жӣІеҰҘзҸ еҚ•жҠ—+PD-L1жҠ‘еҲ¶еүӮпјҲжҒ©жІғеҲ©еҚ•жҠ—пјү+еҢ–з–—ж–№жЎҲз”ЁдәҺHER2йҳіжҖ§д№іи…әзҷҢжӮЈиҖ…зҡ„еӣҪеҶ…дёҙеәҠIIжңҹз ”з©¶еҲҶжһҗпјҢжүҫеҲ°дәҶе…Қз–«жІ»з–—дёҺжҠ—HER2еҚ•жҠ—вҖңдёҚжқҘз”өвҖқзҡ„еҺҹеӣ гҖӮиҜҘз ”з©¶и®әж–ҮеҸ‘иЎЁдәҺгҖҠзҷҢз»ҶиғһгҖӢпјҲCancer CellпјүгҖӮ
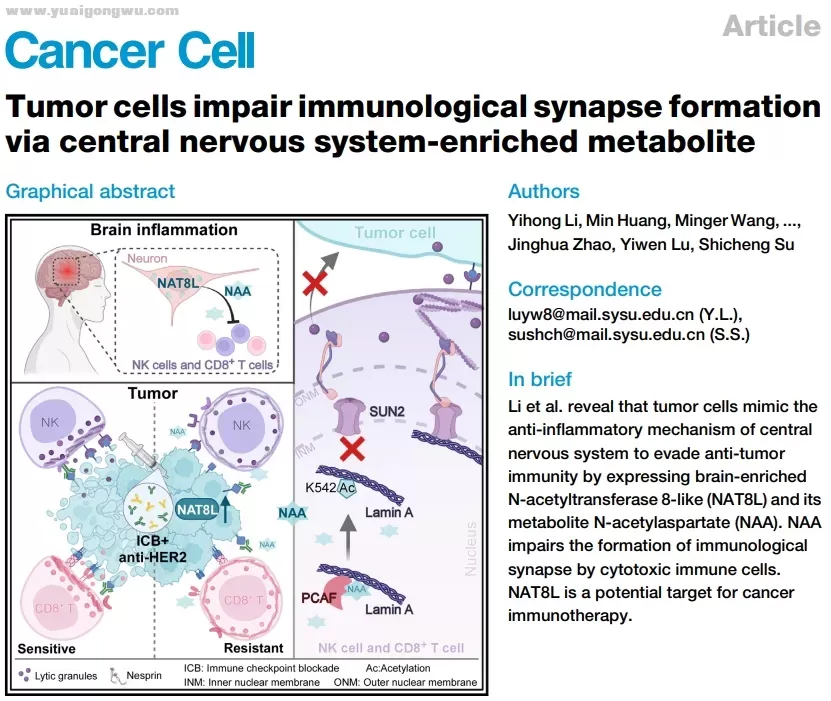
з ”з©¶жҳҫзӨәпјҢз»ҸжӣІеҰҘзҸ еҚ•жҠ—е’ҢPD-L1жҠ‘еҲ¶еүӮжІ»з–—зҡ„HER2йҳіжҖ§д№іи…әзҷҢжӮЈиҖ…иӮҝзҳӨеҶ…пјҢеӯҳеңЁN-д№ҷй…°иҪ¬з§»й…¶8ж ·иӣӢзҷҪпјҲNAT8LпјүеҸҠе…¶д»Ји°ўдә§зү©зҡ„еҜҢйӣҶпјҢе®ғ们жӯЈеёёжғ…еҶөдёӢжҳҜдёӯжһўзҘһз»Ҹзі»з»ҹпјҲCNSпјүеҶ…жҠ‘еҲ¶NKз»Ҷиғһе’ҢCD8+Tз»ҶиғһпјҲдәәдҪ“еҶ…зҡ„дёӨз§Қе…Қз–«з»Ҷиғһпјүзҡ„з»ҶиғһжҜ’жҖ§гҖҒеҮҸиҪ»и„‘йғЁзӮҺз—ҮжҚҹдјӨзҡ„зү©иҙЁпјҢдҪҶеҚҙиў«зҷҢз»Ҷиғһз”ЁжқҘз ҙеқҸе…Қз–«зӘҒи§ҰеҪўжҲҗпјҢиҝӣиҖҢжҠ‘еҲ¶жҠ—иӮҝзҳӨе…Қз–«еә”зӯ”[2]гҖӮ
иҝӣдёҖжӯҘзҡ„еҚ•з»ҶиғһжөӢеәҸжҳҫзӨәпјҢNAT8Lдё»иҰҒз”ұиӮҝзҳӨеҶ…зҡ„зҷҢз»ҶиғһиЎЁиҫҫпјҢдё”дёҺжӮЈиҖ…дёҚиүҜз”ҹеӯҳйў„еҗҺжҳҫи‘—зӣёе…іпјӣе°Ҹйј е®һйӘҢеҲҷжҳҫзӨәпјҢж•ІйҷӨзҷҢз»Ҷиғһзҡ„NAT8Lеҹәеӣ еҸҜжҳҫ著延缓其еңЁе…Қз–«еҒҘе…Ёе°Ҹйј дҪ“еҶ…зҡ„иҝӣеұ•йҖҹеәҰпјҢ并еўһејәPD-L1жҠ‘еҲ¶еүӮе’ҢжӣІеҰҘзҸ еҚ•жҠ—еҚ•зӢ¬дҪҝз”ЁеҸҠиҒ”еҗҲдҪҝз”Ёзҡ„з–—ж•ҲпјҢиҜҙжҳҺNAT8LеҜ№жҠ—иӮҝзҳӨе…Қз–«еә”зӯ”жңүжҳҺжҳҫзҡ„дёҚеҲ©еҪұе“ҚгҖӮ
еҗҢж—¶еҗҺз»ӯе®һйӘҢиҜҒе®һпјҢеңЁж•ІйҷӨNAT8LеҗҺпјҢNKз»Ҷиғһе’ҢCD8+Tз»ҶиғһеҜ№зҷҢз»Ҷиғһзҡ„з»ҶиғһжҜ’жҖ§жқҖдјӨиғҪеҠӣжҳҫи‘—еўһејәпјҢиҝҷд№ҹиҜҙжҳҺNAT8LжҳҜжҠ‘еҲ¶дёӨз§Қе…Қз–«з»ҶиғһеҜ№зҷҢз»ҶиғһжқҖдјӨеҠӣзҡ„е…ій”®гҖӮжӯӨеӨ–пјҢNAT8Lзҡ„д»Ји°ўдә§зү©д№ҹеҸ‘жҢҘдәҶзӣёдјјзҡ„жңәеҲ¶гҖӮ
зҷҢз»Ҷиғһзҡ„иҝҷз§ҚгҖҢе…Қз–«йҖғйҖёгҖҚи·Ҝж•°пјҢзӣёеҪ“дәҺжЁЎжӢҹдәҶеӨ§и„‘жҠ—зӮҺз—Үзҡ„жңәеҲ¶пјҢеұһе®һвҖңзӢЎзҢҫвҖқгҖӮдёҚиҝҮпјҢз ”з©¶еҸ‘зҺ°дәҶNAT8LпјҢе°ҶеҸҜд»ҘдҪңдёәд№іи…әзҷҢжІ»з–—дёӯзҡ„з”ҹзү©ж Үеҝ—зү©д№ғиҮіиҚҜзү©ејҖеҸ‘йқ¶зӮ№пјҢиҝӣдёҖжӯҘеўһејәжҲ‘们еҜ№зҷҢз»Ҷиғһзҡ„еӣҙиҝҪе өжҲӘпјҒ
зҷҢз»ҶиғһйҖҡиҝҮвҖңеҗғйҶӢвҖқпјҢиҝҳиғҪеҗғеҮәжқҘдёӘгҖҢе…Қз–«йҖғйҖёгҖҚиғҪеҠӣ
2024е№ҙ5жңҲпјҢз”ұжөҷжұҹеӨ§еӯҰеҗ•еҝ—ж°‘еӣўйҳҹдёҺеӣҪ家зҷҢз—Үдёӯеҝғиө«жҚ·еӣўйҳҹе…ұеҗҢе®ҢжҲҗзҡ„з ”з©¶пјҢеҸ‘иЎЁеңЁгҖҠиҮӘ然·代谢гҖӢпјҲNature MetabolismпјүдёҠгҖӮз ”з©¶еҸ‘зҺ°пјҡзҷҢз»Ҷиғһд№ҹжҳҜе–ңж¬ўвҖңеҗғйҶӢвҖқзҡ„пјҢиҝҷеҜјиҮҙиӮҝзҳӨз»„з»ҮдёӯCD8+Tз»Ҷиғһжөёж¶ҰеҮҸе°‘пјҢдҝғиҝӣгҖҢе…Қз–«йҖғйҖёгҖҚ[3]гҖӮ
йҶӢй…ёпјҢеҸҲз§°д№ҷй…ёпјҢжҳҜзҹӯй“ҫи„ӮиӮӘй…ёзҡ„йҮҚиҰҒз»„жҲҗжҲҗеҲҶгҖӮдәәдҪ“иЎҖж¶ІеҫӘзҺҜдёӯйҶӢй…ёеҗ«йҮҸжіўеҠЁиҫғеӨ§пјҢзәҰдёә50 ~ 800 ОјMпјҢйҶӢй…ёеҗ«йҮҸдё»иҰҒеҸ—йҘ®йЈҹжҲҗеҲҶеҪұе“ҚпјҲдҫӢеҰӮйЈҹйҶӢгҖҒд№іеҲ¶е“ҒгҖҒеҠ е·Ҙзҡ„иӮүзұ»е’ҢйқўеҢ…гҖҒй…’зІҫеҸҠдёҚжҳ“ж¶ҲеҢ–зҡ„зўіж°ҙеҢ–еҗҲзү©пјүгҖӮ
жң¬йЎ№з ”究дёӯпјҢз ”з©¶иҖ…们еҸ‘зҺ°йҶӢй…ёжҳҜйқһе°Ҹз»ҶиғһиӮәзҷҢпјҲNSCLCпјүдёӯеҗ«йҮҸжңҖй«ҳзҡ„зҹӯй“ҫи„ӮиӮӘй…ёпјҢиҖҢдё”зҷҢз»Ҷиғһж‘„еҸ–йҶӢй…ёзҡ„иғҪеҠӣжҳҺжҳҫеўһејәпјҢеҰӮжһңзҷҢз»ҶиғһжүҖеӨ„зҺҜеўғеҶ…зҡ„и‘Ўиҗ„зі–еҗ«йҮҸдёҘйҮҚдёҚи¶іпјҢйҶӢй…ёе°ұдјҡжҲҗдёәжӣҝд»Јзҡ„иғҪйҮҸжқҘжәҗпјҢдҪҝзҷҢз»Ҷиғһзҡ„еўһж®–йҖҹзҺҮжҳҫи‘—еҠ еҝ«пјҢжҲҗеҠҹеә”еҜ№иғҪйҮҸд»Ји°ўеә”жҝҖгҖӮ
з ”з©¶иҖ…们еҲҶжһҗеҸ‘зҺ°пјҢеӨ–жәҗжҖ§иЎҘе……йҶӢй…ёеҗҺпјҲеңЁи‘Ўиҗ„зі–еүҘеӨәзҺҜеўғдёӢпјүпјҢзҷҢз»ҶиғһеҶ…зҡ„c-MycиӣӢзҷҪж°ҙе№іжҳҺжҳҫдёҠеҚҮгҖҒе…¶еҚҠиЎ°жңҹ延й•ҝгҖӮc-MycжҳҜз»ҶиғһеҶ…йҮҚиҰҒзҡ„иҪ¬еҪ•еӣ еӯҗпјҢc-MycиӣӢзҷҪж°ҙе№ізҡ„дёҠи°ғеёҰеҠЁзҡ„зӣёе…іжңәеҲ¶пјҢеҸҲдјҡдҝғдҪҝзҷҢз»Ҷиғһи¶ҠжқҘи¶ҠвҖңзҲұеҗғйҶӢвҖқпјҢиҖҢиҝҷеҸҲиҝӣдёҖжӯҘеҠ©еҠӣдәҶзҷҢз»Ҷиғһзҡ„е…Қз–«йҖғйҖёе’ҢеҠ йҖҹеўһж®–иғҪеҠӣгҖӮ
еҗҢж—¶пјҢз ”з©¶иҝӣдёҖжӯҘе°ҶеӨ–жәҗжҖ§иЎҘе……йҶӢй…ёеҗҺзҡ„зҷҢз»ҶиғһдёҺе…Қз–«з»ҶиғһпјҲCD8+Tз»Ҷиғһпјүе…ұеҹ№е…»ж—¶пјҢжҸҗзӨәе…Қз–«з»Ҷиғһзҡ„жҝҖжҙ»зҠ¶жҖҒжҳҺжҳҫдёҚдҪізҡ„дҝЎеҸ·пјҢиҝҷж„Ҹе‘ізқҖвҖңеҗғйҶӢвҖқи®©зҷҢз»Ҷиғһе…·жңүдәҶе…Қз–«жҠ‘еҲ¶дҪңз”ЁгҖӮ
иҜҘз ”з©¶е°ҶиҝӣдёҖжӯҘжҢҮеҜјйҖҡиҝҮи°ғиҠӮиӮҝзҳӨйҶӢй…ёд»Ји°ўйҖ”еҫ„еўһејәе…Қз–«з–—жі•зҡ„з–—ж•ҲпјҢ并дёәе…Қз–«жІ»з–—зӣёе…із ”究жү“ејҖдәҶжӣҙеӨҡзӘҒз ҙеҸЈгҖӮ
зҷҢз»ҶиғһгҖҢе…Қз–«йҖғйҖёгҖҚд№ҹжңүвҖңеё®еҮ¶вҖқ
2024е№ҙ2жңҲпјҢзҫҺеӣҪйә»зңҒзҗҶе·ҘеӯҰйҷўз§‘иө«з»јеҗҲзҷҢз—Үз ”з©¶жүҖеңЁгҖҠиҮӘ然гҖӢпјҲ Natureпјү еҲҠж–ҮпјҢйҰ–ж¬ЎжҸӯзӨәдәҶ иҪ¬еҪ•еӣ еӯҗSOX17 еҸҜдҪҝзҷҢз—ҮгҖҢе…Қз–«йҖғйҖёгҖҚпјҢ并且ејәи°ғдәҶйҳ»ж–ӯSOX17еҠҹиғҪжҲ–е…¶жҝҖжҙ»йҖ”еҫ„пјҢжңүжңӣдёәзҷҢз—Үж—©жңҹжІ»з–—еёҰжқҘж–°зҡ„ж–№еҗ‘е’Ңзӯ–з•Ҙ[4]гҖӮ
еңЁзҷҢз—ҮеҸ‘з”ҹеүҚпјҢдёҖиҲ¬дјҡз»ҸеҺҶдёҖдёӘвҖңзҷҢеүҚз—…еҸҳвҖқзҡ„йҳ¶ж®өпјҢиӯ¬еҰӮжҒҜиӮүдёҖиҲ¬иў«з§°д№Ӣдёәз»“зӣҙиӮ зҷҢзҡ„вҖңиҝ‘дәІвҖқпјҢйҖҡеёёиў«и®ӨдёәжҳҜз»“зӣҙиӮ зҷҢзҡ„зҷҢеүҚз—…еҸҳгҖӮ
дёәдәҶдәҶи§ЈеңЁзҷҢз—ҮеҮәзҺ°еүҚпјҢзҷҢз»ҶиғһжҳҜеҰӮдҪ•иҝӣиЎҢгҖҢе…Қз–«йҖғйҖёгҖҚзҡ„пјҢз ”з©¶еӣўйҳҹеҹ№е…»дәҶиҝ·дҪ зүҲзҡ„з»“зӣҙиӮ иӮҝзҳӨпјҢе°Ҷе…¶жӨҚе…ҘеҲ°е°Ҹйј дҪ“еҶ…пјҢеҗҢж—¶и®ҫи®ЎдәҶеңЁдәәзұ»з»“зӣҙиӮ зҷҢдёӯеёёиў«еҸ‘зҺ°зҡ„еҹәеӣ зӘҒеҸҳзұ»еһӢпјҢеҰӮKRAS G12DгҖҒP53зјәеӨұгҖҒAPCзјәеӨұзӯүгҖӮ
еңЁе®һйӘҢе°Ҹйј дҪ“еҶ…пјҢз ”з©¶еӣўйҳҹи§ӮеҜҹеҲ°иӮҝзҳӨдёӯSOX17зҡ„иЎЁиҫҫжҳҫи‘—еўһеҠ пјҢиҜҘеҹәеӣ зј–з ҒжҳҜдёҖз§ҚиҪ¬еҪ•еӣ еӯҗпјҢйҖҡеёёеҸӘеңЁиғҡиғҺеҸ‘иӮІжңҹй—ҙжҙ»и·ғпјҢеё®еҠ©жҺ§еҲ¶иӮ йҒ“еҸ‘иӮІе’ҢиЎҖз®Ўзҡ„еҪўжҲҗгҖӮ
еҗҢж—¶пјҢз ”з©¶еӣўйҳҹиҝӣдёҖжӯҘжҸӯзӨәдәҶеҪ“SOX17еңЁзҷҢз»Ҷиғһдёӯиў«жҝҖжҙ»ж—¶пјҢе®ғдјҡеё®еҠ©еҲӣйҖ дёҖдёӘе…Қз–«жҠ‘еҲ¶еҫ®зҺҜеўғгҖӮе№Іжү°зҙ ОіпјҲIFNОіпјүеҸ—дҪ“жҳҜе…Қз–«зі»з»ҹеҜ№жҠ—зҷҢз»Ҷиғһзҡ„жӯҰеҷЁд№ӢдёҖгҖӮSOX17зҡ„дё»иҰҒдҪңз”Ёд№ӢдёҖжҳҜе…ій—ӯз»“зӣҙиӮ зҷҢз»Ҷиғһе’ҢзҷҢеүҚз—…еҸҳз»Ҷиғһдёӯзҡ„IFNОідҝЎеҸ·йҖҡи·ҜпјҢ然еҗҺзҷҢз»ҶиғһеҸҜд»ҘйҖғйҒҝе…Қз–«з»Ҷиғһзҡ„зӣ‘и§ҶпјҢдёҚж–ӯжҲҗй•ҝпјҢжңҖз»Ҳжј”еҸҳжҲҗзҷҢгҖӮ
иҖҢеңЁж•ІйҷӨSOX17еҹәеӣ еҗҺпјҢз ”з©¶еӣўйҳҹеҸ‘зҺ°е°Ҹйј зҡ„е…Қз–«зі»з»ҹиғҪеӨҹжңүж•Ҳж”»еҮ»иӮҝзҳӨпјҢеҹәжң¬ж¶ҲйҷӨдәҶиӮҝзҳӨз»Ҷиғһзҡ„жҢҒз»ӯз”ҹеӯҳиғҪеҠӣгҖӮиҝҷиЎЁжҳҺпјҢйқ¶еҗ‘жҠ‘еҲ¶SOX17еҸҜиғҪдёәж—©жңҹжІ»з–—з»“иӮ зҷҢжҸҗдҫӣдёҖз§Қж–°ж–№жі•гҖӮ
жӯӨеӨ–пјҢз ”з©¶еӣўйҳҹиҝҳеҲҶжһҗдәҶдәәзұ»з»“зӣҙиӮ зҷҢжӮЈиҖ…зҡ„еҹәеӣ иЎЁиҫҫж•°жҚ®пјҢз»“жһңжҳҫзӨәпјҢSOX17еңЁж—©жңҹз»“зӣҙиӮ зҷҢдёӯй«ҳиЎЁиҫҫпјҢдҪҶдјҡйҡҸзқҖиӮҝзҳӨзҡ„иҝӣеұ•е’ҢиҪ¬з§»иҖҢдёӢйҷҚгҖӮж„Ҹе‘ізқҖпјҢйҡҸзқҖз»“зӣҙиӮ зҷҢиҝӣеұ•е’ҢиҪ¬з§»пјҢиҝҳжңүе…¶д»–жңәеҲ¶еҲӣйҖ дәҶе…Қз–«жҠ‘еҲ¶зҺҜеўғпјҢSOX17зҡ„йҮҚиҰҒжҖ§д№ҹйҡҸд№ӢйҷҚдҪҺгҖӮ
дҪңдёәдёҖз§ҚиҪ¬еҪ•еӣ еӯҗпјҢSOX17иў«и®ӨдёәжҳҜйҡҫжҲҗиҚҜйқ¶зӮ№пјҢеӣ жӯӨз ”з©¶еӣўйҳҹи®ЎеҲ’йҖҡиҝҮиҜҶеҲ«дёҺSOX17зӣёдә’дҪңз”Ёзҡ„е…¶д»–иӣӢзҷҪиҙЁпјҢд»ҺиҖҢжүҫеҲ°жӣҙе®№жҳ“йҳ»ж–ӯе…¶жңәеҲ¶зҡ„ж–№жі•гҖӮжӯӨеӨ–пјҢ他们иҝҳи®ЎеҲ’иҝӣдёҖжӯҘжҺўзҙўи§ҰеҸ‘зҷҢеүҚз»ҶиғһдёӯSOX17еҗҜеҠЁе’Ңй«ҳиЎЁиҫҫзҡ„зӣёе…іжңәеҲ¶гҖӮ
её®еҠ©зҷҢз»ҶиғһгҖҢе…Қз–«йҖғйҖёгҖҚпјҹз ҙи§ЈиҝҷдёӘйқ¶зӮ№жңүжңӣе®һзҺ°еҜ№зҷҢз—ҮвҖңеҸҢйҮҚжү“еҮ»вҖқ
SMARCAL1д№ҹиў«и§ҶдҪңжҳҜдёҖдёӘжңүеүҚйҖ”зҡ„иӮҝзҳӨе…Қз–«жІ»з–—ж–°йқ¶зӮ№гҖӮ
2024е№ҙ1жңҲпјҢе“ҘдјҰжҜ”дәҡеӨ§еӯҰ欧ж–ҮеҢ»еӯҰдёӯеҝғзҡ„з ”з©¶дәәе‘ҳеңЁгҖҠз»ҶиғһгҖӢпјҲ Cellпјү жңҹеҲҠеҸ‘иЎЁзҡ„и®әж–ҮжҳҫзӨәпјҢDNAжҚҹдјӨеә”зӯ”еӣ еӯҗSMARCAL1йҖҡиҝҮдёӨз§Қдә’иЎҘжңәеҲ¶дҝғиҝӣзҷҢз»ҶиғһгҖҢе…Қз–«йҖғйҖёгҖҚгҖӮйқ¶еҗ‘жҠ‘еҲ¶SMARCAL1иғҪеӨҹиҜұеҜјзҷҢз—ҮиҮӘдё»е…Қз–«дҝЎеҸ·пјҢеҗҢж—¶дёӢи°ғPD-L1ж°ҙе№іпјҢе®һзҺ°еҜ№зҷҢз—Үзҡ„вҖңеҸҢйҮҚжү“еҮ»вҖқпјҢдә§з”ҹжӣҙеҘҪзҡ„жІ»з–—ж•Ҳжһң[5]гҖӮ
иҜҘйЎ№з ”з©¶дёӯпјҢз ”з©¶еӣўйҳҹйҖҡиҝҮзӣёе…іеҹәеӣ з»„зӯӣйҖүпјҢеҸ‘зҺ°SMARCAL1жҳҜдёҖдёӘжңүеҲ©дәҺиӮҝзҳӨе…Қз–«йҖғйҖёзҡ„еӣ зҙ пјҢе…¶йҖҡиҝҮеҸҢйҮҚжңәеҲ¶вҖ”вҖ”жҠ‘еҲ¶еӣәжңүе…Қз–«дҝЎеҸ·гҖҒиҜұеҜјPD-L1д»ӢеҜјзҡ„е…Қз–«жЈҖжҹҘзӮ№еҸҚеә”пјҢеё®еҠ©зҷҢз»ҶиғһгҖҢе…Қз–«йҖғйҖёгҖҚгҖӮ
д»ҺжңәеҲ¶дёҠи®ІпјҢSMARCAL1йҷҗеҲ¶еҶ…жәҗжҖ§DNAжҚҹдјӨпјҢд»ҺиҖҢеңЁзҷҢз»Ҷиғһз”ҹй•ҝиҝҮзЁӢдёӯжҠ‘еҲ¶зӣёе…іе…Қз–«дҝЎеҸ·иҪ¬еҜјгҖӮеҗҢж—¶пјҢе®ғеңЁPD-L1иҪ¬еҪ•и°ғиҠӮе…ғ件дёҠдҝқжҢҒжҹ“иүІиҙЁеҸҜеҸҠжҖ§пјҢд»ҺиҖҢдҝғиҝӣзҷҢз»ҶиғһдёӯPD-L1зҡ„иЎЁиҫҫгҖӮ
еңЁй»‘иүІзҙ зҳӨе°Ҹйј жЁЎеһӢдёӯпјҢйҖҡиҝҮж•ІйҷӨSMARCAL1пјҢз ”з©¶иҖ…еҸ‘зҺ°жҠ‘еҲ¶дәҶдёҠиҝ°дёӨз§ҚзҷҢз»Ҷиғһе…Қз–«йҖғйҖёзҡ„иғҪеҠӣпјҢеўһејәдәҶжҠ—иӮҝзҳӨе…Қз–«еҸҚеә”пјҢ并дҪҝе°Ҹйј еҜ№е…Қз–«з–—жі•жӣҙеҠ ж•Ҹж„ҹгҖӮ
иҝҷдәӣеҸ‘зҺ°зЎ®е®ҡдәҶSMARCAL1дҪңдёәжҠ—иӮҝзҳӨе…Қз–«зҡ„и°ғиҠӮеҷЁпјҢжҳҜдёҖдёӘе…·еӨҮжҪңеҠӣзҡ„зҷҢз—Үе…Қз–«жІ»з–—ж–°йқ¶зӮ№гҖӮ
е°Ҹз»“
д»ҺгҖҢе…Қз–«йҖғйҖёгҖҚиҝ‘еҮ е№ҙжүҖеҸ—еҲ°е…іжіЁе’Ңеҗ„з§ҚдёҚеҗҢзҡ„з ”з©¶еҸҜд»ҘзңӢеҲ°пјҢзҷҢз»ҶиғһзңҹжҳҜеӨ§еӨ§ж»ҙвҖңзӢЎзҢҫвҖқпјҢдјҡд»Ҙеҗ„з§ҚдёҚеҗҢзҡ„зӯ–з•ҘпјҢдҪҝдәәдҪ“зҡ„е…Қз–«зі»з»ҹеҸ—еҲ°жҠ‘еҲ¶пјӣдёҚиҝҮпјҢдәәзұ»еңЁе…Қз–«з–—жі•дёҠзҡ„дёҚж–ӯзӘҒз ҙпјҢд№ҹжҳҜжҳҫиҖҢжҳ“и§Ғзҡ„гҖӮ
жҖ»иҖҢиЁҖд№ӢпјҢвҖңзҢ«жҠ“иҖҒйј вҖқзҡ„ж•…дәӢд»ҚйңҖ继з»ӯпјҢдҪҶеҫҲеӨҡз ”з©¶ж–№еҗ‘д№ҹжҳҜи§Ұзұ»ж—ҒйҖҡзҡ„пјҢжүҫеҲ°зӣёдјјзҡ„жңәеҲ¶пјҢеҸ‘жҺҳзӣёе…ізҡ„йқ¶зӮ№пјҢ然еҗҺеҶҚз ”з©¶жҳҺзҷҪжҖҺд№Ҳз”ЁеҘҪе®ғгҖӮеңЁдәәзұ»зҡ„еҸ‘еұ•еҸІдёҠпјҢжҲ‘们жӣҫжҲҳиғңдәҶж— ж•°з—…з—ӣпјҢжүҖд»ҘпјҢд№ҹеҗҢж ·иҰҒзӣёдҝЎпјҢе…Қз–«з»ҶиғһжңҖз»ҲиғҪеӨҹе°ҶзҷҢз»ҶиғһдёҖдёӘдёӘвҖңе°ұең°жӯЈжі•вҖқпјҒ
еҸӮиҖғж–ҮзҢ®
[1]Huober J, Barrios C H, Niikura N, et al. Atezolizumab with neoadjuvant antiвҖ“human epidermal growth factor receptor 2 therapy and chemotherapy in human epidermal growth factor receptor 2вҖ“positive early breast cancer: primary results of the randomized phase III IMpassion050 trial[J]. Journal of Clinical Oncology, 2022, 40(25): 2946-2956.
[2]Li Y, Huang M, Wang M, et al. Tumor cells impair immunological synapse formation via central nervous system-enriched metabolite[J]. Cancer Cell, 2024.
[3]Wang J, Yang Y, Shao F, et al. Acetate reprogrammes tumour metabolism and promotes PD-L1 expression and immune evasion by upregulating c-Myc[J]. Nature Metabolism, 2024.
[4]Goto N, et al. SOX17 enables immune evasion of early colorectal adenomas and cancers. Nature. 2024 Feb 28.
9жңҲзҰҸеҲ©
ж–Үз« еЈ°жҳҺпјҡжң¬ж–ҮдёӯжүҖж¶үеҸҠзҡ„дҝЎжҒҜж—ЁеңЁдј йҖ’еҢ»иҚҜеүҚжІҝдҝЎжҒҜе’Ңз ”з©¶иҝӣеұ•пјҢдёҚж¶үеҸҠиҜҠз–—ж–№жЎҲжҺЁиҚҗпјҢдёҙеәҠдёҠиҜ·йҒөд»ҺеҢ»з”ҹжҲ–е…¶д»–еҢ»з–—еҚ«з”ҹдё“дёҡдәәеЈ«зҡ„ж„Ҹи§ҒдёҺжҢҮеҜјгҖӮ